Glioxal
Glioxala OCHCHO formulako konposatu organikoa da dialdehidoen familiakoa bi aldehido talde baititu egituran. Solido kristalinoa zuria da tenperatura baxuetan, baina horitu egiten da fusio-puntura hurbiltzean (15º C). Likidoa horia da eta lurrundurik berdea.
| Glioxal | |
|---|---|
 | |
| Formula kimikoa | C2H2O2 |
| SMILES kanonikoa | 2D eredua |
| MolView | 3D eredua |
| Konposizioa | oxigeno eta karbono |
| Mota | biogenic acyclic aldehyde (en) |
| Ezaugarriak | |
| Fusio-puntua | 15 °C |
| Irakite-puntua | 50,4 °C (101,325 kPa) |
| Masa molekularra | 58,005 Da |
| Arriskuak | |
| NFPA 704 | |
| Identifikatzaileak | |
| InChlKey | LEQAOMBKQFMDFZ-UHFFFAOYSA-N |
| CAS zenbakia | 107-22-2 |
| ChemSpider | 7572 |
| PubChem | 7860 |
| Reaxys | 1732463 |
| Gmelin | 34779 |
| ChEMBL | CHEMBL1606435 |
| ZVG | 28700 |
| EC zenbakia | 203-474-9 |
| ECHA | 100.003.160 |
| CosIng | 34157 |
| MeSH | D006037 |
| RxNorm | 4967 |
| Human Metabolome Database | HMDB0303107 |
| KNApSAcK | C00059081 |
| UNII | 50NP6JJ975 |
| KEGG | C14448 |
| PDB Ligand | GXT |
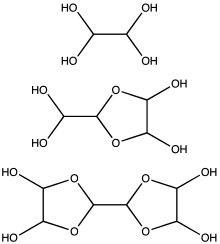
Glioxal hutsa izatea ez da ohikoa hidratatu eta oligomeroak eratzen dituelako. Hala ere, horrek ez du arazorik sortzen bere erabilera askotarako[1][2].
Glioxala aztarna-gas moduan agertzen da atmosferan hidrokarburoen oxidazioz sortua[3].
Produkzioa
aldatuHeinrich Debus kimikari alemanak prestatu zuen lehen aldiz glioxala etanola azido nitrikoz erreakzionaraztean[4].
Bi manera daude glioxal komertziala prestatzeko[1]:
- etilen glikola gas moduan oxidatuz zilar- edo kobre-katalizatzaile bat usatuz,
- edo azetaldehido likidoa azido nitrikoz oxidatuz,
Glioxal komertziala normalean % 40ko ur-disoluziotan saltzen da.
Erabilera
aldatuGlioxala kuxe papera egiteko eta ehungintzako akabera-prozesuetan baliatzen da, zimurtzen ez diren oihalak lortzeko, etsenplurako[1].
Polimeroen kimikan disolbatzaile eta saretze-agente moduan erabiltzen da.
Kimika organikoan konposatu konplexuagoak sintetizatzeko lehengai moduan baliatzen da, imidazolaren moduko heterozikloak sintetizatzeko adibidez.
Histologian finkatzaile moduan usatzen da.
Erreferentziak
aldatu- ↑ a b c (Ingelesez) Karpov, Andrey; Walsdorff, Christian; Siemer, Michael; Mattioda, Georges; Blanc, Alain. (2021). «Glyoxal» Ullmann's Encyclopedia of Industrial Chemistry (John Wiley & Sons, Ltd): 1–11. doi:. ISBN 978-3-527-30673-2. (Noiz kontsultatua: 2021-11-28).
- ↑ (Ingelesez) PubChem. «Glyoxal» pubchem.ncbi.nlm.nih.gov (Noiz kontsultatua: 2021-11-28).
- ↑ (Ingelesez) Vrekoussis, M.; Wittrock, F.; Richter, A.; Burrows, J. P.. (2009-07-14). «Temporal and spatial variability of glyoxal as observed from space» Atmospheric Chemistry and Physics 9 (13): 4485–4504. doi:. ISSN 1680-7316. (Noiz kontsultatua: 2021-11-28).
- ↑ (Ingelesez) Debus, H. (1857). "On glyoxal. Philosophical Magazine, 4th series, 13, 66. or..
