Erribonukleasa
Erribonukleasa, RNAasa edo RNasa ere deitua, RNA makromolekularen hidrolisia katalizatzen duen entzima (nukleasa) da. Bi talde nagusitan sailkatu daiteke, alde batetik endonukleasak daude; beste aldetik exonukleasak eta hainbat azpimaila biltzen dituzte EC 3.1 entzima klaseen barruan.
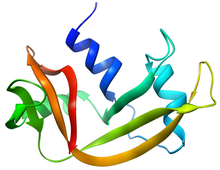
Erribonukleasak oso ohikoak dira, ondorioz, babesik gabeko ingurunetan RNA molekulen bizitza murriztea dakartze. DNA molekulen babeserako erribonukleasen inhibitzaileak (IR) erabiltzen dira, zeintzuek zelulako proteinen proportzio handia hartzen duten (~%0,1) eta erribonukleasei (RNAsei) beste edozein proteina-proteina elkarrekintza baino afinitate gehiagorekin lotzen zaien; egoera fisiologiko normalean IR-RNAsa A konplexuaren disoziazio konstanteak -20 fM-ko balioa dauka. IR molekulak oso erabiliak dira RNA molekulen ikerketan aritzen diren laborategietan; izan ere, IR proteinei esker RNA inguruko erribonukleasetatik babestuta egongo da.
Harrigarria bada ere, erribonukleasen apurketa-sekunztiak hauskorrak izaten dira. Ez dira DNA harizpi bikoitza sekuentzia espezifikoetan ebakitzen dituzten errestrikzio entzimen analogoak. DNA harizpi bikoitza sekuentzia espezifikoetan mozteko ezgaitasun hori gainditzeko, RNAasa H eta moztu nahi den DNA sekuentziaren harizpi osagarria baino ez da beharrezkoa.
RNAasek hainbat prozesu biologikoetan garrantzitsuak diren funtzioak betetzen dituzte, hain zuzen ere, angiogenesia eta loredun landareen (angioespermak) auto-konpatibilitatea.
Erlazionatutako ikerketak
aldatuEukariotoen artean bi erribonukleasa H aurkitu daitezke: RNAasa H1 eta RNAasa H2 [1]. RNAasa H2 hiru azpiunitatez osatutako konplexu multimerikoa da: RNAasa H2A, RNAasa H2B eta RNAasa H2C[2]. DNA duplexeko erribonukleotidoa ezagutu eta bere 5’-fosfodiester lotura apurtuz RNA katea digeritzen du[3]. Hiru genek parte hartzen dute RNAasa H2 molekularen sintesian eta hauetan mutazioak agertzen direnean hiru geneetan Aicardi-Goutieres (AGS) sindrome erresezibo autosomikoa pairatu daiteke (RNAasa H2 molekularen funtzio partzialaren galera)[4].
Reijns-en 2012ko ikerketan, [5] saguen RNAasa H2b genearen mutagenesia burutu zen. Ikerketaren helburua ugaztunen RNAasa H2 entzimaren rola ikustea izan zen. Izan ere, RNAasa H2b genearen erauzketak enbrio-hilgarritasun goiztiarra eragiten du saguetan. Ikerlarien hipotesiaren arabera, saguen hazkuntzaren geldialdia DNA genomikoko erribonukleotidoen pilaketak p53ren menpeko DNAan eragindako kaltearen ondorioz gertatzen da.↵Hurrengo informazioa eztabaidatzen da ikerketan:
- Erribonukleotidoak RNAasa H2 gene mutatuak dituzten zeluletan pilatzen dira, DNA polimerasaren jardueraren ondorioz. Bestalde, autoreek, erribonukleotidoen inkorporazioak metazooetan ere gertatzen direla erakusten dute eta lesio hauek ugaztunen zelulentzat kaltegarriak direla diote, haien desagerpen funtsezkoa izanik sagu enbrionarioen garapenerako. Modu berean, alkalirekiko sentikorrak diren zonaldeak bereizten dira: kalteak DNA genomikoan kobalenteki txertatutako erribonukleotido sinple edo bikoitzek eragindakoak dira. Erribonukleotido hauek zelulako 1.000.000 tokitan txertatzen dira, hots, ugaztunen genomako akats endogeno ohikoena da. Kalte hauek erreplikazioko polimerasen txertaketa akatsdunaren bitartez ere aldatu daizteke.
- RNAsa H2, erribonukleotidoen eliminaziorako beharrezkoa den genomaren zaiketarako entzima da. Entzima honetan mutazio bat pairatzen zuten saguen DNA genomikoan erribonukleotidoen pilaketak, genomaren osotasuna mantentzeko RNAsa H2 entzimaren garrantzia erakusten du. Akumulazio kaltegarri honek, hidrolisiaren ondoko fosfodiester loturaren sentikortasuna aregotzen da erribosaren 2’-hidroxilo muturrean. Ikerketak dioenez, 7.600 nukleotidotik behin erribonukleotidoak inkorporatzen dira, zelulako 1.300.000 lesio eraginez.
- Gaixki txertatutako erribonukleotidoek DNAn kalteak eragiten dituzte: ez da erribonukleotidoek erreplikazioa oztopatzen dutela, DNA polimerasak erribonukleotidodun moldeekin lan egin dezakete, embriogenesi goiztiar normalarekin. Arazoa, gehiegizko erribonukleotido kantitateak azaltzen direnean ematen da. DNAn kalteari erantzuten dion seinalizazioa, erribonukleotidoak erreplikatzeko zailak diren guneetan txertatzen direnean ematen dela uste da. Bestalde, kromosomen berrantolaketak aurkitu dira: DNAn apurketak, erreplikazio konplexuetan emandako arazoen edo kontrako DNA katetako erribonukleotidoen hidrolisiaren ondorioz eman daitezkeenak. Gainera, DNAan akatsak p53-ak gidatutako proliferazioaren inhibizioa eragin dezake enbrioietan, eta ondorioz, enbrioiaren heriotza suposatu.
- Erribonukleotidoen txertaketak osasunean eta gaixotasunetan daukan eragina: kantitate txikian erribonukleotidoen txertaketak jasangarriak dira. Izan ere, ARNasa H2ren mendekoak ez diren konponketa bideen bitartez sortutako azido nukleikoen substratu aberratzaileak, sortzetiko erantzun immunea ematen dutela uste da. Bestalde, erribonukleotidoek DNAn sortutako kalteen ondoriozko seinalizazioa eragin dezakete, jarrian interferonen sintesia estimulatu dezakeena.
- Laburbilduz, ikerketa honetan, ugazkunentzat erribonukleotidoak oso kaltegarriak izan daitezkeela esaten da Izan ere, genomaren ezegonkortasuna eragin dezakete. Bestalde, RNAasa H2 entzima RNA genomikoaren osotasuna mantentzeko ezinbestekoa dela azaltzen du. Horrez gain, erribonukleotidoek DNA genomikoan pizten dituzten seinalizazio bideak aipatzen ditu. Hau guztia jakinda, DNA genomikoan erribonukleotidoek dituzten funtzio patologiko eta fisiologikoak hobeto uler daitezke, bai azido nukleikoetan oinarritutako autoinmunitatean, bai kartzinogenesian.
Erreferentziak
aldatu- Cerritelli, Susana M.; Crouch, Robert J.. (2009-02-18). «Ribonuclease H: the enzymes in eukaryotes» FEBS Journal 276 (6): 1494–1505. doi:10.1111/j.1742-4658.2009.06908.x. ISSN 1742-464X. (Noiz kontsultatua: 2022-03-31).
- Crow, Y. J.; Rehwinkel, J.. (2009-10-06). «Aicardi-Goutieres syndrome and related phenotypes: linking nucleic acid metabolism with autoimmunity» Human Molecular Genetics 18 (R2): R130–R136. doi:10.1093/hmg/ddp293. ISSN 0964-6906. (Noiz kontsultatua: 2022-03-31).
- Chon, Hyongi; Vassilev, Alex; DePamphilis, Melvin L.; Zhao, Yingming; Zhang, Junmei; Burgers, Peter M.; Crouch, Robert J.; Cerritelli, Susana M.. (2008-11-16). «Contributions of the two accessory subunits, RNASEH2B and RNASEH2C, to the activity and properties of the human RNase H2 complex» Nucleic Acids Research 37 (1): 96–110. doi:10.1093/nar/gkn913. ISSN 1362-4962. (Noiz kontsultatua: 2022-03-31).
- Crow, Yanick J; Hayward, Bruce E; Parmar, Rekha; Robins, Peter; Leitch, Andrea; Ali, Manir; Black, Deborah N; van Bokhoven, Hans et al.. (2006-07-16). «Mutations in the gene encoding the 3′-5′ DNA exonuclease TREX1 cause Aicardi-Goutières syndrome at the AGS1 locus» Nature Genetics 38 (8): 917–920. doi:10.1038/ng1845. ISSN 1061-4036. (Noiz kontsultatua: 2022-03-31).
- (Ingelesez) Reijns, Martin A. M.; Rabe, Björn; Rigby, Rachel E.; Mill, Pleasantine; Astell, Katy R.; Lettice, Laura A.; Boyle, Shelagh; Leitch, Andrea et al.. (2012-05-25). «Enzymatic Removal of Ribonucleotides from DNA Is Essential for Mammalian Genome Integrity and Development» Cell 149 (5): 1008–1022. doi:10.1016/j.cell.2012.04.011. ISSN 0092-8674. (Noiz kontsultatua: 2022-03-31).